Вакцина от аллергии, запускающая выработку антител против иммуноглобулина E, успешно прошла первые доклинические испытания: в экспериментах на мышах она предотвращала местную аллергическую реакцию, а также анафилактический шок при внутривенном введении аллергена. При этом препарат никак не повлиял на способность иммунитета защищать животных от паразитарной инфекции. Исследование опубликовано в Science Translational Medicine.

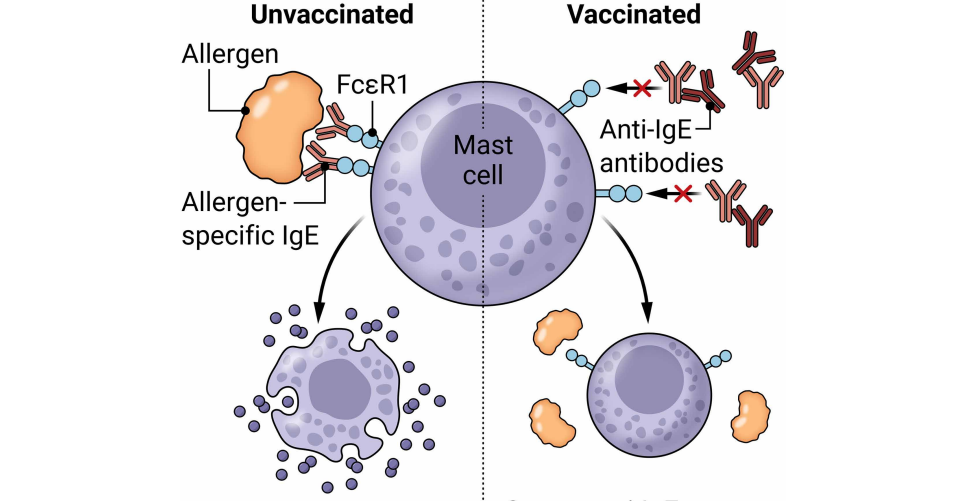
При аллергии происходит чрезмерная активация тучных клеток, которая проявляется высыпаниями на коже, зудом, насморком, а в тяжелых случаях доходит до анафилактического шока. Он развивается из-за резкого высвобождения содержимого гранул тучных клеток и может привести к смерти из-за отека дыхательных путей и падения артериального давления. Тучные клетки активируются под воздействием иммуноглобулина E (IgE), поэтому ученые используют IgE как мишень при создании лекарств от аллергии. Например, для терапии больных уже применяют моноклональные антитела (омализумаб), которые связываются с иммуноглобулином E, но такое лечение пока доступно ограниченному числу пациентов из-за высокой цены на препарат и необходимости вводить его многократно.
Группа исследователей под руководством Лорана Ребера (Laurent L. Reber) из Тулузского института инфекционных и воспалительных заболеваний предположила, что для долгосрочной защиты от аллергии можно провакцинировать пациента от иммуноглобулина E. Исследователи создали конъюгированную вакцину IgE-K, в которой содержится фрагмент человеческого IgE, связанный с белком CRM197 для увеличения иммуногенности. В ответ на введение препарата иммунная система вырабатывает антитела против IgE. Связываясь с IgE, они препятствуют активации тучных клеток.
Для испытания вакцины ученые создали гуманизированную линию мышей, у которых IgE и его рецептор соответствуют человеческому. Животным ввели три дозы препарата, вызвавшего выработку антител против IgE с высоким титром по сравнению с контрольной группой, которую вакцинировали только белком CRM197 (p < 0,001).
Затем у мышей спровоцировали развитие аллергии, введя им аллергены как местно, так и системно. При местном введении у мышей экспериментальной группы наблюдали пониженную дегрануляцию тучных клеток по сравнению с контрольной группой (p < 0,01). При внутривенном (системном) введении препарата у животных из контрольной группы температура тела снизилась в среднем на три градуса, что говорит об анафилактической реакции. У животных, вакцинированных экспериментальным препаратом, изменений в физиологических показателях не было (p < 0,001).
Антитела против IgE в крови у мышей сохранялись до года после вакцинации. Препарат не вызывал видимых побочных реакций, а также не влиял на защитный иммунитет животных при гельминтной инфекции Strongyloides ratti: статистически значимой разницы между числом тучных клеток и количеством ДНК паразита в кишечнике животных не было. Все это делает вакцину многообещающим средством для предотвращения аллергии, но несмотря на первые успехи в доклинических исследованиях, вакцине предстоит еще доказать свою эффективность и безопасность для людей.
Недавно мы рассказывали о том, что ученые разобрались в причинах анафилактического шока при пищевой аллергии: он обусловлен генетическим вариантом фермента, разрушающего лейкотриен D4.


